Class 9 Science Chapter 2 क्या हमारे आस-पास के पदार्थ शुद्ध हैं? इस अध्याय में हम शुद्ध और अशुद्ध पदार्थों की विशेषताओं को समझते हैं। यह अध्याय हमें मिश्रण, विलयन और विभिन्न पृथक्करण विधियों के बारे में जानकारी देता है। यहाँ हम सरल भाषा में इस अध्याय के मुख्य बिंदुओं और महत्वपूर्ण प्रश्नों पर चर्चा करेंगे।
Class 9 Science Chapter 2 क्या हमारे आस-पास के पदार्थ शुद्ध हैं? हिन्दी में नोट्स
| पाठ्यपुस्तक | NCERT |
| कक्षा | कक्षा 9 |
| विषय | विज्ञान |
| अध्याय | अध्याय 2 |
| प्रकरण | क्या हमारे आस-पास के पदार्थ शुद्ध हैं? |
Class 9 Science Chapter 2 क्या हमारे आस-पास के पदार्थ शुद्ध है?
पदार्थ (Matter):
पदार्थ एक प्रकार का द्रव्य है जो कि भौतिक प्रक्रमों द्वारा अन्य प्रकार के द्रव्य में पृथक नहीं किया जा सकता है। एक शुद्ध पदार्थ एक ही प्रकार के कोणों से बना होता है।
शुद्ध पदार्थ क्या है?
जिस पदार्थ में केवल एक ही प्रकार के कण होते हैं, वह शुद्ध पदार्थ कहलाता है।
उदाहरण: शुद्ध पानी, शुद्ध नमक, ऑक्सीजन गैस।
✍ शुद्ध शब्द का अर्थ होता है पदार्थ में कोई मिलावट न हो, परंतु एक वैज्ञानिक भाषा में सभी वस्तुएँ विभिन्न पदार्थों के मिश्रण है। अतः शुद्ध नहीं है। उदाहरण के लिए – जल, दूध, वसा इत्यादि।
✍ शुद्ध पदार्थ से तात्पर्य है कि उस पदार्थ में मौजूद सभी कण समान रासायनिक प्रकृति के होते है।
✍ एक शुद्ध पदार्थ एक ही प्रकार के कणों से मिलकर बना होता है।
मिश्रण (Mixture) क्या होता है?:
वह पदार्थ जो दो या दो से अधिक तत्वों या यौगिकों को किसी भी अनुपात में परस्पर मिला देने से प्राप्त होता है, मिश्रण कहलाता है । मिश्रण के अवयवों को सरल यांत्रिक विधियों द्वारा पृथक किया जा सकता है । उदाहरण – हवा, समुद्री जल, दूध, इस्पात आदि मिश्रण के उदाहरण हैं ।
मिश्रण के प्रकार (Types of mixture):
मिश्रण दो प्रकार के होते हैं।
1. समांगी मिश्रण (Homogenous mixture)
2. विषमांगी मिश्रण (Heterogenous mixture)
1. समांगी मिश्रण (Homogenous mixture):
जब किसी मिश्रण के अवयव सम्पूर्ण मिश्रण में समान रूप से फैले होते है अर्थात मिश्रण में स्थित अवयवों का मिश्रण के प्रत्येक भाग में अनुपात समान होता है तो मिश्रण, समांगी मिश्रण कहलाता है । जैसे- चीनी और जल का मिश्रण एक समांगी मिश्रण हैं।
2. विषमांगी मिश्रण (Heterogenous mixture)
जब किसी मिश्रण के अवयव सम्पूर्ण मिश्रण में समान रूप से फैले न हो अर्थात मिश्रण में स्थित अवयवों का मिश्रण के प्रत्येक भाग में अनुपात समान न हो, तो इस प्रकार के मिश्रण को विषमांगी मिश्रण कहते हैं । जैसे- शक्कर (चीनी) और बालू (रेत) का मिश्रण एक विषमांगी मिश्रण है।
◆ विषमांगी मिश्रण में, उसके पूरे द्रव्यमान में एक-सा संघटन नहीं होता है।
◆ द्रवों में ठोसों के निलम्बन (Suspension) भी विषमांगी मिश्रण है।
🔷 विलयन (Solution):
विलयन दो या दो से अधिक पदार्थों का समांगी मिश्रण होता है। उदाहरण- नींबू जल, सोडा जल, चीनी जल आदि विलयन के उदाहरण है।
◆ किसी विलयन को दो भागों में अर्थात विलायक (solvent) और विलेय (solute) में बांटा जाता है।
◆ विलयन का वह घटक जो दूसरे घटक को विलयन में मिलाता है, उसे विलायक (solvent) कहते हैं।
◆ विलयन का वह घटक जो विलायक में घुला रहता है उसे विलेय (solute) कहते हैं ।
उदाहरण- चीनी और जल के विलयन में चीनी विलेय और जल विलायक है।
🌟 विलयन के गुण (Properties of Solution):
| गुण | विवरण |
|---|---|
| 1️⃣ समांगी मिश्रण | इसका हर हिस्सा एक जैसा दिखाई देता है |
| 2️⃣ कण नहीं दिखते | घुले हुए कण आँखों से नहीं दिखते |
| 3️⃣ फिल्टर नहीं होता | इसे फिल्टर से अलग नहीं किया जा सकता |
| 4️⃣ पारदर्शी (Transparent) | अधिकतर विलयन पारदर्शी होते हैं |
| 5️⃣ स्थायी होता है | लंबे समय तक रखने पर परतें नहीं बनती |
🧮 विलयन की सांद्रता (Concentration of Solution):
विलयन की सांद्रता यह बताती है कि उसमें घुलनशील पदार्थ की मात्रा कितनी है।
📌 दो प्रकार की सांद्रता:
- अधिक सांद्र विलयन (Concentrated Solution):
जिसमें ज्यादा मात्रा में घुलनशील पदार्थ हो।
👉 जैसे – बहुत मीठा चीनी पानी - कम सांद्र विलयन (Dilute Solution):
जिसमें कम मात्रा में घुलनशील पदार्थ हो।
👉 जैसे – हल्का मीठा पानी
🧪 सांद्रता मापने का तरीका (Formula):

या
सांद्रता = (घुलनशील पदार्थ की मात्रा / विलयन की कुल मात्रा) × 100
👉 उदाहरण: अगर 5 ग्राम नमक को 100 ग्राम पानी में घोला जाए, तो
सांद्रता = (5/105) × 100 = लगभग 4.76%
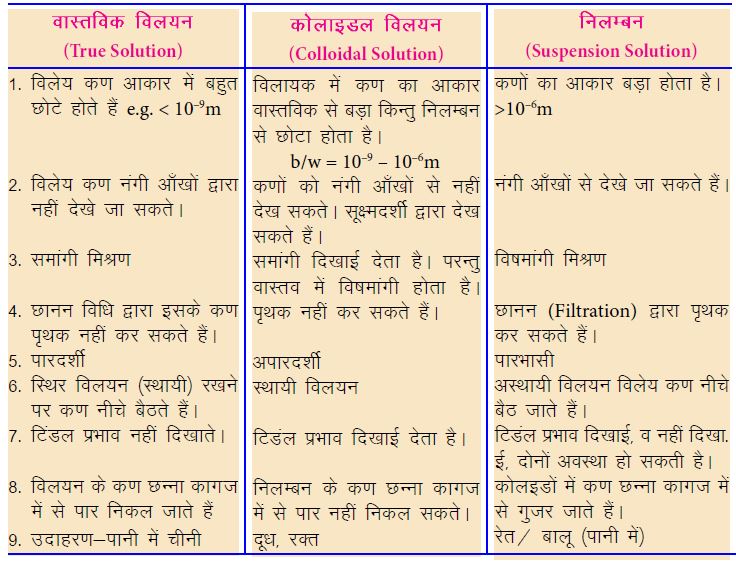
विलयन के प्रकार (Types of Solution):
🔷 कोलॉइड क्या है? (What is Colloid)
कोलॉइड एक ऐसा मिश्रण होता है जिसमें घुले हुए कण बहुत छोटे होते हैं, परंतु वे विलयन के कणों से बड़े होते हैं और पूरे घोल में फैले रहते हैं।
✅ उदाहरण:
- दूध 🥛
- धुंध 🌫️
- झाग 🫧
- मक्खन 🧈
- क्रीम
📌 कोलॉइड के गुण:
| गुण | विवरण |
|---|---|
| 1️⃣ समांगी दिखाई देता है | पर वास्तव में विषमांगी होता है |
| 2️⃣ कण नग्न आँखों से नहीं दिखते | लेकिन माइक्रोस्कोप से देखे जा सकते हैं |
| 3️⃣ टिण्डल प्रभाव दिखाता है | प्रकाश की किरण परिक्षेपित होती है |
| 4️⃣ फिल्टर से अलग नहीं किया जा सकता | क्योंकि कण बहुत छोटे होते हैं |
| 5️⃣ स्थिर होता है | समय के साथ कण नीचे नहीं बैठते |
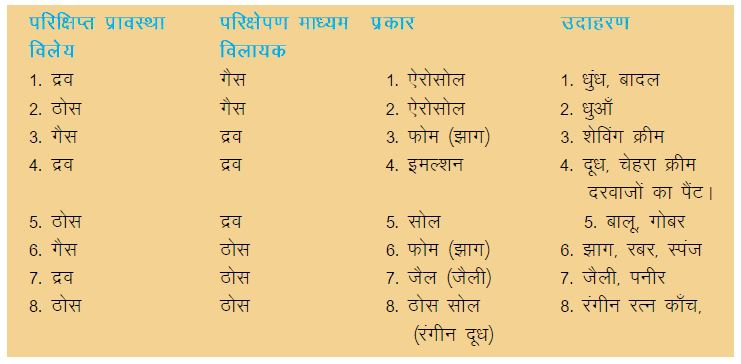
कोलाईड्स विलयन के कुछ सामान्य उदाहरण (Common examples of colloids)
🌟 टिण्डल प्रभाव (Tyndall Effect):
जब कोलॉइड पर प्रकाश डाला जाता है, तो कण प्रकाश को बिखेरते हैं और उसकी किरणें स्पष्ट दिखाई देती हैं।
👉 जैसे – धूप में धूल या कोहरे के कणों को देखना।
🔷 निलंबन क्या है? (What is Suspension in Hindi)
निलंबन (Suspension) एक ऐसा मिश्रण होता है जिसमें घुले हुए कण इतने बड़े होते हैं कि वे तरल के अंदर तैरते रहते हैं और समय के साथ नीचे बैठ जाते हैं।
✅ उदाहरण:
- मिट्टी + पानी का घोल
- चॉक पाउडर + पानी
- रेत + पानी
📌 निलंबन के गुण:
| गुण | विवरण |
|---|---|
| 1️⃣ विषमांगी मिश्रण | कण पूरे घोल में समान रूप से नहीं फैले होते |
| 2️⃣ कण नग्न आंखों से दिखाई देते हैं | क्योंकि कण बड़े होते हैं |
| 3️⃣ फिल्टर से अलग किया जा सकता है | जैसे – छानकर रेत अलग करना |
| 4️⃣ अस्थिर होता है | कण समय के साथ नीचे बैठ जाते हैं |
| 5️⃣ टिण्डल प्रभाव दिखा सकता है | यदि कणों का आकार सही हो |
🔄 विलयन, कोलॉइड और निलंबन की तुलना (Table):
| गुण | विलयन (Solution) | कोलॉइड (Colloid) | निलंबन (Suspension) |
|---|---|---|---|
| मिश्रण का प्रकार | समांगी | विषमांगी | विषमांगी |
| कणों का आकार | बहुत छोटा | मध्यम | बड़ा |
| कण दिखते हैं? | नहीं | नहीं (पर माइक्रोस्कोप से) | हां |
| फिल्ट्रेशन संभव? | नहीं | नहीं | हां |
| टिण्डल प्रभाव | नहीं | हां | संभवतः हां |
| स्थायित्व | स्थिर | स्थिर | अस्थिर |
मिश्रण को पृथक करने के तरीके (Methods of Seperation of Mixture):
वाष्पीकरण (Evaporation):
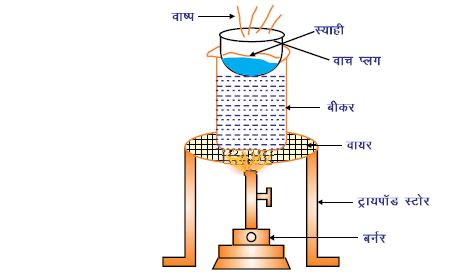
मूल उद्देश्य – मिश्रण के दो पदार्थों में से एक पदार्थ का वाष्पीकरण होना (जैसे एक पदार्थ का क्वथनांक दूसरे से कम होता है।)
सामग्री – रंग डाई (जिसका क्वथनांक ज्यादा हैं) तथा पानी बीकर, वॉच ग्लास । जब हम पानी में मिले रंग को गर्म करते हैं तो पानी वाष्पित हो जाता है तथा रंग वाच गिलास में रह जाता है।
अपकेंद्रीकरण (Centrifugation):
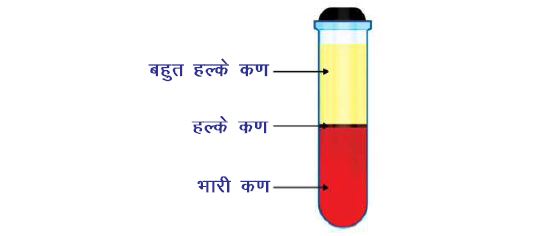
मूल उद्देश्य (सिद्धांत) – जब किसी पदार्थ को तेजी से घुमाया जाता है तो भारी कण नीचे की तरफ दबाव डालता हैं तथा हल्का कण ऊपर चले जाता हैं। उदाहरण – दूध से क्रीम पृथक करना । (क्या तुम जानते हो कि टोंड दूध तथा डबल टोंड दूध किसे कहते हैं?)
◆ शराब (Wine) तथा रक्त को जांचने के लिए प्रयोगशाला में इस्तेमाल किए जाते हैं।
◆ क्रीम से मक्खन बनाने में ।
◆ वाशिंग मशीन में कपड़ों से पानी निकालने के लिए इसी विधि का उपयोग किया जाता है ।
(क्या आपने देखा है कि हमारे कपड़ों से निकले धूल और मिट्टी के कण वाशिंग मशीन में नीचे बैठ जाता हैं। आप जानते हैं ऐसा क्यों?)
पृथक्करण कीप (Deferential entraction funnel):
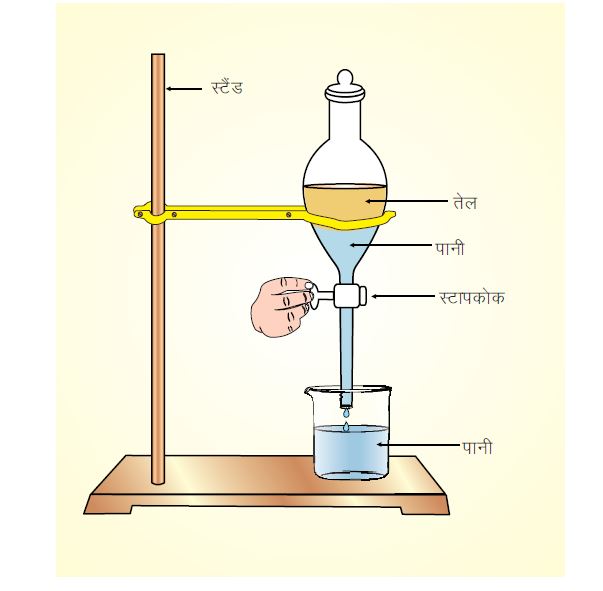
मूल सिद्धांत – दो अघुलनशील द्रव (जो दोनों एक साथ नहीं खुल सकते) को आसानी से पृथक्करण कीप द्वारा अलग कर सकते हैं।
पृथक्कारी कीप का स्टॉप कार्क खोलने से पानी दूसरे बीकर में इकट्ठा कर सकते हैं तथा दूसरे बीकर में बचा तेल इकट्ठा कर सकते हैं।
अनुप्रयोग (Application)
◆ पानी से तेल पृथक करना
उर्ध्वपातन विधि (Sublimation):
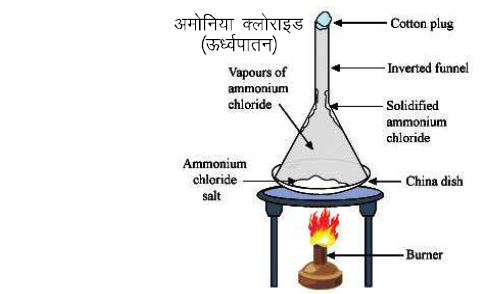
मूल सिद्धांत – दो पदार्थों के बीच एक पदार्थ ऊर्ध्वपातीत हो जाता है (सीधे ठोस से गैस में परिवर्तित हो जाना) जबकि दूसरा ऐसे ही रहता है
उदाहरण – अमोनियम क्लोराइड (NH4Cl) तथा खाने का नमक के मिश्रण को आसानी से अलग किया जा सकता है । मिश्रण को गर्म करने पर अमोनियम क्लोराइड सीधे ठोस से गैस बन जाता है जबकि नमक शेष रह जाता है । अनुप्रयोग (Application):
कपूर, नेफ्थलिन की गोलियां, आयोडीन, अमोनियम क्लोराइड ऊर्ध्वपातन द्वारा अलग हो जाता हैं।
क्रोमेटोग्राफी (Chromatography):
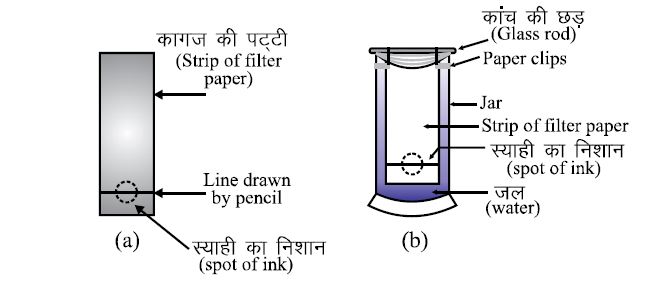
मूल सिद्धांत – किसी मिश्रण में रंगीन यौगिक, रंजित कणों को पृथक कर सकते हैं । किसी सोखने वाले फिल्टर पेपर की सहायता से जब पानी (या किसी भी विलयन) के कण ऊपर की ओर दो अलग-अलग रंग के साथ जाता हैं तो क्रोमेटोग्राफी पेपर द्वारा दोनों पृथक हो जाता जाता हैं क्योंकि दोनों रंग अलग-अलग गति से सोख लिए जाते हैं।
काली सिहाई में उपस्थित रंगों को क्रोमेटोग्राफी द्वारा पृथक करना
अनुप्रयोग (Application):
◆ रंगों (डाई) को पृथक करने के लिए ।
◆ क्लोरोफिल से रंजक (Pigment) पृथक करने के लिए ।
◆ खून से ड्रग पृथक करने में ।
(क्या आप सोच सकते हैं कि जब किसी खिलाड़ी का डोपिंग टेस्ट होता है तो खून का क्या करते हैं?)
आसवन विधि (Distillation):
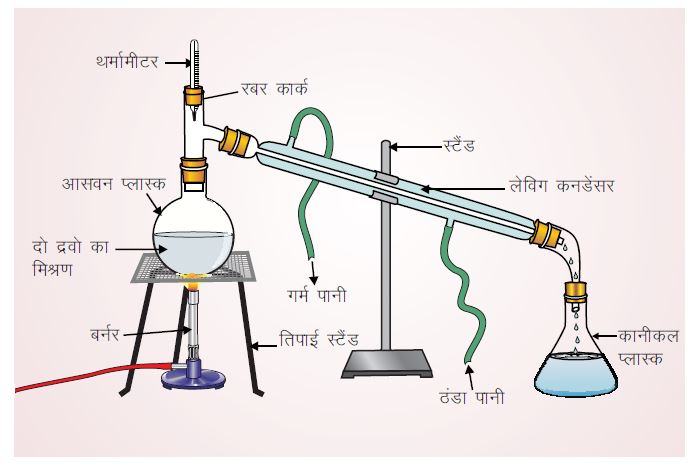
मूल सिद्धांत – दो संघटकों (Component) के बीच एक का क्वथनांक दूसरे से कम होता है।
यह विधि दो या दो से अधिक घुलनशील द्रवों को अलग करने के लिए किया जाता है ।
उदाहरण – जब पानी और एसीटोन के मिश्रण को गर्म किया जाता है, (क्योंकि एसीटोन का क्वथनांक (Boiling Point) कम होता है), यह गर्म होकर वाष्पित होकर ट्यूब में चला जाता है जहां यह फिर द्रव बन जाता है । इस प्रकार एसीटोन बीकर में एकत्र हो जाता है जबकि पानी फ्लास्क में ही रह जाता है ।
नोट (Note) – अगर दो संघटक एक ही द्रव में उपस्थित होते हैं (जिनका क्वथनांक भिन्न होता है) तब हम प्रभाजी आसवन विधि का इस्तेमाल करते हैं ताकि सारे संघटक अलग-अलग हो जाए, उदाहरण हवा तथा पेट्रोलियम आदि ।
पेट्रोलियम को पैरोफिन मोम तेल, स्नेहक, डीजल, केरोसिन, पेट्रोल तथा पेट्रोल गैस को इस विधि द्वारा पृथक किया जाता है ।

साधारण प्रभाजी स्तंभ एक नली होती है जो शीशे के गुटको से भरी होती है । ये गुटके वाष्प को ठंडा व संघ संघनित होने के लिए सतह प्रदान करती है
प्रभाजी आसवन विधि के अनुप्रयोग (Some Application of fractional Distillation)
◆ तेल को शुद्ध करने वाली मशीनों द्वारा क्रूड आयल क्रूड आयल अलग करने में ।
◆ कार्बनिक तरल को शुद्ध करने में ।
◆ ऑक्सीजन, द्रव नाइट्रोजन तथा आर्गन को वायु से पृथक करने में प्रभावी आसवन विधि का प्रयोग किया जाता है ।
क्रिस्टलीकरण (Crystallisation)
मूल सिद्धांत – किसी मिश्रण से अशुद्धियों को दूर करने के लिए पहले किसी उपयुक्त विलयन में घोलना और क्रिस्टलीकरण द्वारा एक संघटक को पृथक करना ।
उदाहरण – अशुद्ध कॉपर सल्फेट के क्रिस्टल को पहले सल्फ्यूरिक अमल में घोलते हैं और फिर गर्म करके विलयन को पृथक किया जाता है । जो विलयन बना था उसे पूरी रात रखकर छोड़ दिया जाता है, अतः केवल शुद्ध कॉपर सल्फेट के क्रिस्टल बनते हैं जबकि अशुद्धियां सल्फ्यूरिक अम्ल में ही रह जाती है । इस विलयन को फिल्टर पेपर की सहायता से छीन लिया जाता है और शुद्ध क्रिस्टल प्राप्त कर लिया जाता है ।
वाष्पीकरण से क्रिस्टलीकरण क्यों अधिक बेहतर है?
✍ वाष्पीकरण से क्रिस्टलीकरण निम्न कारणों से उत्तम है –
◆ कुछ ठोस विघटित हो जाते हैं या कुछ गर्म करने पर चीनी के समान झुलस जाते हैं।
◆ छानने के पश्चात भी अशुद्ध विलेय पदार्थ को विलायक में घोलने पर विलयन में कुछ अशुद्धियां रह सकती है।
◆ वाष्पीकरण होने पर ये अशुद्धियाँ ठोस को संदूषित कर सकती है।
उपयोग –
◆ समुद्री पानी से नमक को साफ (या शुद्ध) करना।
◆ क्रिस्टल को पृथक (शुद्ध) करना (उदाहरण कॉपर सल्फेट (नीला थोथा), फिटकरी, (जिनके क्रिस्टल में अशुद्धियां विद्यमान होती है ।)
◆ जल घर या निकाय में जल को शुद्ध करना (Water Purification in water treatment Plants)

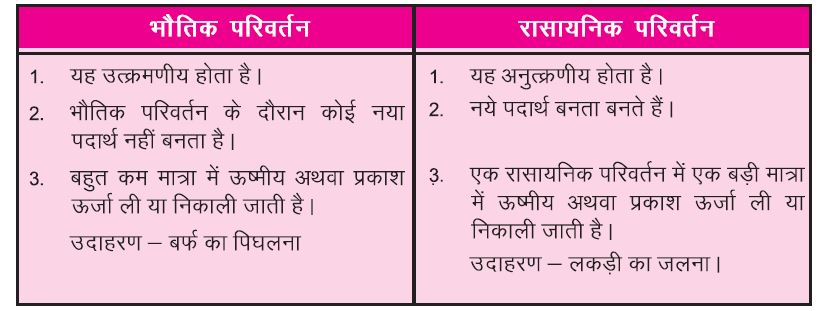
भौतिक तथा रासायनिक परिवर्तन (Physical and Chemical Changes)
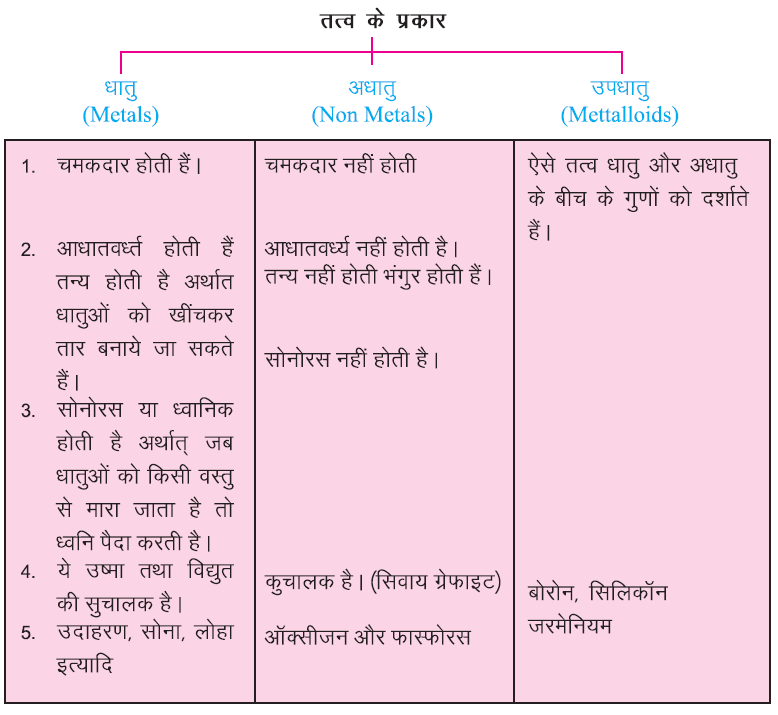
तत्व (Elements)
एक शुद्ध पदार्थ जिसे ना तो साधारण पदार्थों में तोड़ा जा सके ना ही किसी ज्ञात भौतिक व रासायनिक क्रिया द्वारा दो या साधारण पदार्थों से बनाया जा सके, उसे तत्व कहते हैं; जैसे – लोहा, सोडियम आदि ।
✍ तत्व एक ही प्रकार के अणुओं से मिलकर बने होते हैं ।
तत्व के प्रकार (Types of Elements)
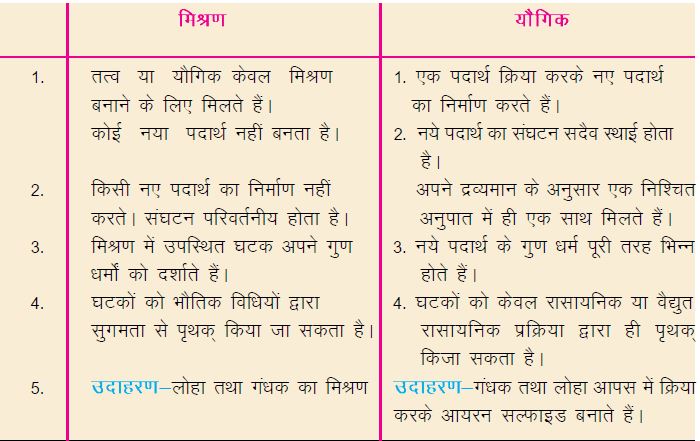
मिश्रण तथा यौगिक में अंतर (Difference between Mixture and Compound)